Korrektur 03.10.2021 bei Fehler im Flowchart: Reduktion des Insulin auf 0,05IE / kg / h!
Da wir in letzter Zeit gehäuft Fälle von diabetischer Ketoazidose auf unserer Intensivstation hatten, folgt hier quasi tagesaktuell die Aufarbeitung des Themas.
Unmittelbare Ursache ist immer ein akuter relativer oder absoluter Mangel an Insulin, der zu einer schweren – auch lebensbedrohlichen – Stoffwechselentgleisung und kardiovaskulären Instabilitäten führt.
Coma diabeticum wird die sich entwickelnde Bewusstseinseinschränkung genannt, aber nur etwa 10% der Patienten sind tatsächlich nach GCS- und neurologischen Scores wirklich bewusstlos. Eher sind sie bewusstseinseingeschränkt. Dennoch muss hier natürlich zielstrebig gehandelt werden.
Wie kommt es überhaupt zu dem Insulinmangel?
In weiteren 25% der Fälle ist die Ketoazidose ein Ausdruck einer Erstmanifestation eines Typ 1 Diabetes. Dann sollte sich die übliche Diabetesdiagnostik anschließen (im Zweifel: internistisches Konsil anfordern).
In ~40% der Fällen, und damit am häufigsten!, ist eine Infektion der Auslöser, der den Stoffwechsel aus den Angeln hebt. Denkt an Pneumonie, Harnwegsinfekt und dergleichen. Bei allem, was man bei der Ketoazidose machen kann – spätestens, wenn man sie im Griff hat, sollte man nach Ursachen suchen, am besten schon parallel.
Weitere Ursachen können sein:
- Ungenügende Insulininjektion bei bekannten Diabetikern
- technische Fehler der Insulinpumpe
- Traumata wie Operation, Unfall
- Gravidität (alles Stressstoffwechsel!)
- Herzinfarkt
- Hyperthyreose
- Therapie mit Saluretika, Kortikosteroiden.
Durch den Insulinmangel kommt es zu einem intrazellulären Glukosemangel. Insulin führt durch die Aktivierung seines Rezeptors zur Aufnahme von Glukose in die Zellen. Bei Mangel müssen die Zellen hungern. Infolgedessen aktiviert sich der bekannte Hungerstoffwechsel mit Lipolyse, Ketonkörperbildung wie Aceton, Acetaldehyd und beta-Hydroxybutyrat (die Biochemie lässt grüßen). Diese Ketone führen zu einer Azidose im Serum, die wiederum den restlichen Stoffwechsel aus den Socken hauen kann (führt jetzt ein wenig zu weit).
Die Kussmaul-Atmung lässt grüßen
Im Rahmen der Ketose kommt es zu der berühmt-berüchtigten Kussmaul-Atmung (schnell und tief): Der Patient hat eine metabolisch bedingte Azidose und versucht sie respiratorisch zu kompensieren. Er hyperventiliert. Das hängt zusammen über
CO2 + H2O <> H2CO3 <> HCO3– + H+
Das über die Azidose anfallende CO2 möchte er schnell weg bekommen. Es wird in der BGA deshalb ein außerordentlich niedriges CO2 auffallen. Bitte nicht dieses CO2 behandeln, sondern die metabolische Azidose! Ich hab leider schon erlebt, dass nur der erste offensichtlich auffällige Werte behandelt wurde. Wenn man aber in dieser Situation die Hyperventilation behandelt, bringt man den Patienten völlig zur Dekompensation. ‚Nuff said.
Übrigens gibt es ein schönes Akronym für die Ursachen der Kussmaul-Atmung:
- K – etone
- U – urämie
- S – epsis
- S – salicylate
- M – ethanol
- A – aldehyde
- U – (rämie)
- L – aktat
Weiterhin herrscht im Zustand einer Ketoazidose ein größerer extrazellulärer Volumenmangel vor.
Aus all diesen pathogenetischen Überlegungen leitet sich unsere Therapie ab.
Der Diagnose folgt die Therapie
Zunächst einmal muss man erkennen, dass es sich um eine Ketoazidose handelt, wenn der Patient somnolent zur Tür reinkommt. Das erste, was auffallen wird, ist wohl die Hyperglykämie. Wenn er dann noch somnolent ist, wird zügig eine BGA veranlasst, die uns dann schon genauere Hinweise gibt: Ausgeprägte Hypokapnie wegen der Kussmaul-Atmung und Azidose.
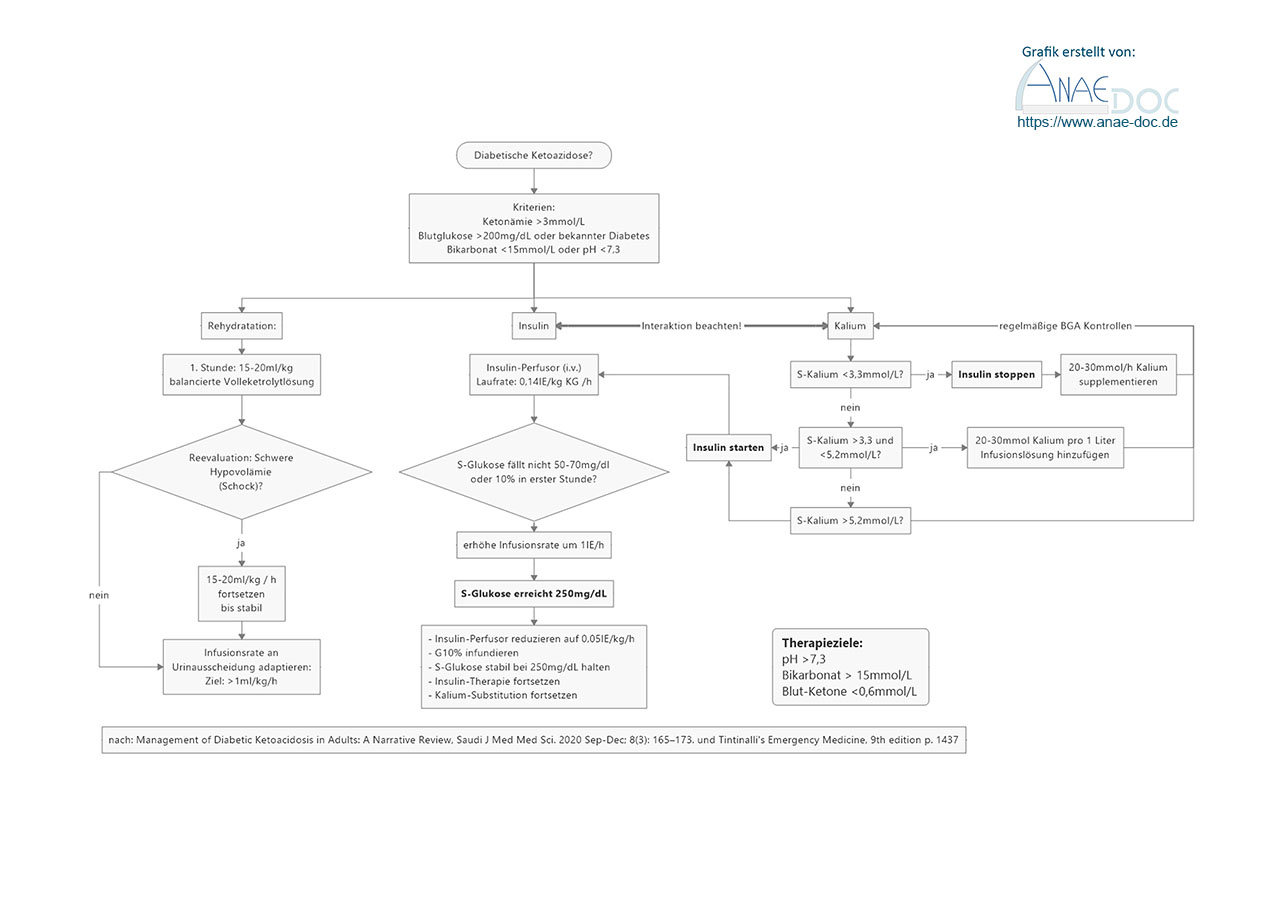
Diagnostische Kriterien sind dann:
- Ketonämie >3mmol/L oder signifikante Ketonurie (U-Status!)
- Blutglukose >11mmol/L (200mg/dL) oder bekannter Diabetes mellitus
- Bikarbonat <15mmol/L und / oder pH <7,3
(nach [2])
Die Ziele der Therapie sind kurz zusammengefasst:
- Ausgleich des Volumendefizits (Reduktion der S-Hyper-Osmolalität, Verbesserung der Perfusion)
- Unterbindung der Ketogenese
- Stoffwechsel-Rekompensation mit Insulin und Elektrolyten (Kalium!)
- Untersuchung auf auslösende Grunderkrankungen
Volumentherapie mit Infusionslösungen
Das Volumendefizit beträgt in den ersten 24 Stunden typischerweise 5-6 Liter. Anfänglich sollte mehr Volumen infundiert werden: 1000ml Vollelektrolytlösung frei, gefolgt von hohen Infusomat-Laufraten (durchaus bis zu 15-20ml/kg/h), dabei Orientierung an der Urinausscheidung. Die Zielportionen liegen bei 1ml/kg KG/h.
Die folgende Insulintherapie führt ihrerseits zu einem intrazellulären Shift von Wasser, und kann somit wieder zu einem extrazellulären Volumenmangel und Verschlechterung der Hypernatriämie führen. Erschwerend kommt hinzu, dass die wahre Natrium-Konzentration bei Hyperglykämie höher ist, als im Labor gemessen.
Als Infusionslösung bitte kein NaCl verwenden, sondern ausschließlich balancierte Vollelektrolytlösungen. Bei den erforderlichen Infusionsmengen kann man eine hyperchlorämische Azidose (Hyperchlorämie) auslösen; und der Patient ist ja schon azidotisch!
Sobald die Glukose-Spiegel unter 250mg/dl fallen, sollte Glukose 10% zur Infusionslösung hinzugefügt werden, um Hypoglykämien zu vermeiden und die Insulintherapie fortsetzen zu können.
Insulintherapie als Schlüssel-Ansatz
Insulintherapie ist ein gutes Stichwort: Insulin führt zu Aufnahme von Glukose in die Zellen und unterbricht den Hungerstoffwechsel. Dazu werden in verschiedenen Quellen unterschiedliche Therapieregimes empfohlen.
Grundsätzlich kann man Insulin sowohl s.c. als auch i.v. verwenden. Bei kritische kranken Patienten sollte aber die i.v.-Route aufgrund der besseren Steuerbarkeit über Perfusor bevorzugt werden[3].
In manchen Quellen wird eine initiale Bolusgabe von 0,1IE/kg KG empfohlen, gefolgt von einer Dauerinfusion (z.B. Herold, Tintinalli). Die unten beschriebenen Risiken sind aber nicht zu verachten und ein „sachteres“ Vorgehen ist gerechtfertigt:
Insulin-Perfusor mit Laufrate 0,14IE / kg KG / h
Die zwei Gefahren dieser Therapie sind Hypoglykämie und Hypokaliämie: beides wird durch Insulin in die Zelle befördert. Außerdem werden im Lauf der Therapie weniger Ketone produziert und die Serum-Azidose lässt nach.
Die Insulintherapie sollte erst starten, wenn das Kalium >3,3mmol/L liegt. Danach Gabe von 20-30mmol Kalium pro 1000ml Infusionslösung[3]. Kalium sollte wiederum erst supplementiert werden, wenn es unter 5,5mmol/L gefallen ist.
Dass man regelmäßig, z.B. halbstündig BGAs durchführen sollte, um die Therapie zu leiten, versteht sich von selbst. Gerade das Kalium-Problem kann schwere Folgen haben, die man frühzeitig erkennen sollte.
Wann sind wir fertig?
Zielwerte der Therapie sind:
- pH > 7,3
- Bikarbonat > 15mmol/L
- Blut-Ketone < 0,6mmol/L
(nach [2])
Man wird sehen, dass sich innerhalb von ein paar Stunden die Imbalancen rekompensieren werden. Es schließt sich dann die Ursachenforschung an.
Links:
- [1]Management of Diabetic Ketoacidosis in Adults: A Narrative Review, Saudi J Med Med Sci. 2020 Sep-Dec; 8(3): 165–173.
- [2]Joint British Diabetes Societies guideline for the management of diabetic ketoacidosis
Begeisterter Anästhesist mit Faible für Teaching und Medizininformatik.






1 Kommentar
2 Pings
Gute Zusammenfassung! Zwei Punkte würde ich ergänzend aufgreifen, da diese einen Diabetologen erfahrungsgemäß oft gefragt werden:
– Stellenwert von NaBic in der Therapie der Azidose bei DKA: Keine Gabe von NaBic, da dies die Gefahr der Hypokaliämie erhöht und keine kausale Therapie darstellt. Der pH wird unter der Therapie von alleine steigen. Ausnahmen sind natürlich sehr schwere Azidosen von 250 mg/dl nicht zutrifft. Die Patienten benötigen in der Regel 2-3 Tage Hohe Dosen Glukose und Insulin, bis man die im Beitrag definierten Zielkriterien erreicht.
Grüße aus Bochum 🙂
[…] eine Diabetische Ketoazidose scheint ein Trigger sein zu können. Da schließt sich der Kreis hier im Blog wieder […]
[…] einer normalen diabetischen Ketoazidose ist ja die Hyperglykämie, wie auch schon auf diesem Blog beschrieben. In diesem Fall fehlte sie, aber es handelte sich trotzdem um eine diabetische Ketoazidose. […]