Manchmal kommt man zum Nachtdienst auf die Intensivstation, bekommt Patienten vorgestellt, und stolpert dann über Dinge, die dem Tagdienst irgendwie durch die Lappen gegangen sind. Einen solchen Fall möchte ich heute mit euch aufbauen. Und nebenbei könnte es sein, dass das zugrunde liegende Krankheitsbild in Zukunft häufiger zu sehen ist, auch wenn es für mich eher ein Kolibri war. Nachdem ich mal auf die Lösung gekommen war.
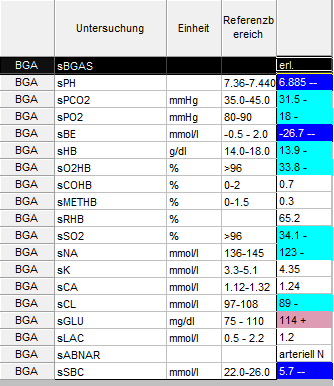
Situation: mitt-50-jähriger Alkohol-kranker Patient mit Leberinsuffizienz und pankreoprivem Diabetes, sowie Panzytopenie (alkohol-toxische Knochenmarkschädigung?) wurde aufgenommen in einer fulminanten Azidose: pH 6,885 – Base Excess -26,7 – Bikarbonat (SBC) 5,7!
Gehen wir doch mal der Reihe nach durch. Wir haben Azidose, offensichtlich. Da das pCO2 normwertig mit 31,5 und das Bikarbonat massiv erniedrigt war, handelte es sich offensichtlich um eine nicht-kompensierte metabolische Azidose. Ein weiterer Hinweis darauf war der deutlich negative Base Excess.
Erstaunlicherweise war das Kalium normwertig trotz der krassen Azidose. Wenigstens ein Problem weniger, um das wir uns kümmern mussten.
Der Patient war etwas somnolent und ihm war übel. Ansonsten entwickelte er relativ schnell nach Aufnahme eine Kussmaul-Atmung, mit der er es sogar auf einen pH von bis zu 7,2 brachte, bei CO2 von 11 😉 Aber das ist auf Dauer ja auch keine Lösung. Das Bikarbonat war einfach viel zu niedrig.
Aber was jetzt tun?
Berechnung der Anionenlücke
Berechnen wir doch einmal die Anionenlücke (dAG = delta Anion-gap):
Na – (Cl+HCO3-)
123 – (89+5,7) = 28,3
Laut Flexikon liegt der Normwert der Anionenlücke bei 3-11mmol/L. Hier hatten wir eine massive Erhöhung. Das lag natürlich zum einen am massiv reduzierten Bikarbonat. Zum anderen lag aber der Verdacht auf eine Additionsazidose nahe. Also zusätzliche Säuren, die in der Anionenlücken-Berechnung nicht erfasst waren.
Der erste Gedanke ist dabei bei mir immer: Laktat. Allerdings war das ja bereits mitbestimmt und normwertig bei 1,2mmol/L. Schade. Nächster Versuch. Das Labor war fertig:
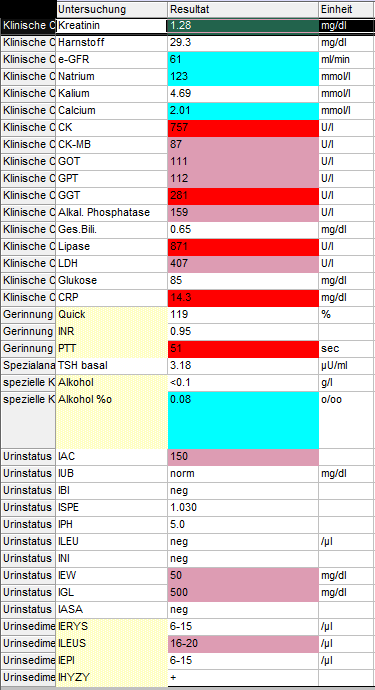
Was man auch hätte erwarten können, wäre vielleicht ein massives Nierenversagen gewesen. Keine Protonenausscheidung mehr, so Dinge eben. Auch das hätte eine Kussmaul-Atmung verursachen können, und auch das hätte das Bikarbonat reduziert. Aber mit einem Kreatinin von 1,28mg/dl doch eher nicht die Ursache.
Auffällig waren erhöhte Leber- und Pankreasenzyme. Leber vermutlich im Rahmen der Alkoholkrankheit, und Pankreas a.e. sogar aufgrund einer akuten Pankreatitis. Das Calcium war mit 2,01 auch schon eher auf der niedrigen Seite, das sollte auch mal supplementiert werden.
Das KUSSMAUL Akronym
Aber jetzt haben wir immer noch keine Idee, was hier los ist. Gehen wir doch noch einmal das Akronym KUSSMAUL durch:
K – etone, U – rämie, S – epsis, S – Salicyliate, M – ethanol, A – ldehyde, L – aktat.
Sepsis- oder Urämiezeichen hatte der Patient nicht, Laktat auch nicht. Vergiftungen waren zumindest „mal eben schnell“ nicht so auszuschließen. Aber Ketone wären doch eine Idee. Deshalb noch schnell einen U-Status hinterher geschoben.
Und siehe da: IAC steht für Aceton – keine Ahnung, wer sich diese Abkürzung in unserem Labor ausgedacht hat. Treffer. Ketoazidose.
Weiterhin auffällig: Im U-Status war die Glukose massiv erhöht (hier bei 500mg/dl), wobei sie im Serum normwertig war mit 85mg/dl. Wie kam das jetzt zustande? Das ist doch physiologisch gar nicht möglich. Ich meine – Nierenschwelle, hallo ?!
Was für Medikamente nimmt der Patient?
Es lohnte sich ein Blick in die Medikamentenliste des Patienten. Zur Therapie seines Diabetes war dort Jardiance verordnet. Das ist Empagliflozin, ein SGLT2-Inhibitor: Sodium-Glukose-linked-Transporter 2. In der Niere. Das Mittel führt also zu einer Glukosurie (q.e.d.) und Natriurie, und ist ein relativ modernes Mittel gegen Diabetes. Es wirkt auch unabhängig von Insulin oder anderen Mechanismen, die beim Diabetes beeinträchtigt sein können. Schönes Mittel.
Soweit, so gut. Der beobachtete Glukose-Effekt wird also eher keine Ursache für die Azidose sein. Allerdings könnte man auf die Idee kommen „Ketoazidose SGLT2“ zu googlen. Und dann wird man ein Wunder erleben.
Offensichtlich können diese Wirkstoffe eine sogenannte euglykäme diabetische Ketoazidose auslösen.
Markenzeichen einer normalen diabetischen Ketoazidose ist ja die Hyperglykämie, wie auch schon auf diesem Blog beschrieben. In diesem Fall fehlte sie, aber es handelte sich trotzdem um eine diabetische Ketoazidose. Verrückte Sache.
Was ist die Ursache?
Zwei Ursachen können zu dem atypischen Bild beitragen.
Zum einen handelte es sich um einen Alkoholiker mit Leber- und Pankreasschaden. Der akute Insulinmangel durch die Pankreasbeteiligung würde normalerweise mit einer Erhöhung der Glukoneogenese in der Leber einhergehen (ein frustraner Versuch, doch noch Glukose in die Zelle zu bekommen über eine Konzentrationserhöhung). Das ging aber nicht, weil die Leber auch geschädigt war (keine Glukoseproduktion). Diese Entität wurde bereits 1973 von Munro beschrieben, dass sie genau Alkoholiker mit Diabetes treffen kann.
Hinzu kommt aber noch der SGLT2-Inhibitor, der alleine genau dasselbe verursachen kann. Es werden verschiedene Mechanismen diskutiert:
- Stimulation von pankreatischen alpha-Zellen und Freisetzung von zu viel Glukagon
- Verminderte renale Ausscheidung von b-Hydroxybutyrat / Acetoacetat
Damit haben wir doch eine Diagnose. Die Therapie ist im Grunde simpel. Wir müssen uns noch nicht mal um die exzessiv hohen Blutglukosespiegel und deren langsame Senkung kümmern (osmotisches Hirnödem durch zu schnelle Senkung).
Allerdings herrscht dennoch ein Insulinmangel vor und die Zellen hungern. Das heißt, wir müssen denen etwas zu fressen anbieten und mit Insulin dafür sorgen, dass es auch in den Zellen ankommt. Bedeutet: Langsam einen Insulinperfusor anlaufen lassen und gleichzeitig Glukose supplementieren, flankiert von regelmäßigen BGA-Kontrollen.
Und wir erinnern uns: Vor allem das Kalium wird sinken und muss ggf. ersetzt werden. Zum einen wegen der Korrektur der Azidose und zum anderen wegen der Insulintherapie.
Zum anderen wird auch das Phosphat über denselben Mechanismus absinken. Die Supplementierung ist nicht zwingend, es sei denn, der Patient zeigt Zeichen der peripheren Erschöpfung (v.a. der Atempumpe oder myokardiale Dysfunktion) oder der Wert ist absolut unter 0,32mmol/L [1]
Ende gut, alles gut
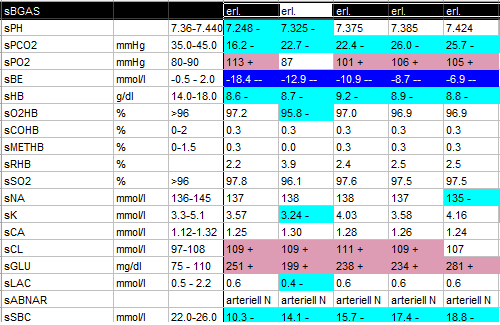
Bei unserem Patienten konnten wir die Ursache erkennen und durch Insulin behandeln (Dosis 0,5IE Insulin/h). In unter 24 Stunden hatten sich die BGAs nahezu normalisiert und die Ketonausscheidung im Urin war fast verschwunden.
Hattet ihr das auch schon mal? Wenn man weiß, wonach man suchen muss, scheint es dann doch gar nicht mehr so selten zu sein (in der DMW erschien 2021 ein Artikel mit der Überschrift „Euglykäme Ketoazidose – Ein Kolibri, der zur Taube werden könnte“. Ich glaube, das trifft es ganz gut.
Links:
- https://news-papers.eu/?p=9012
- [1]Bewusstseinsstörung, Tachypnoe und Tachykardie bei einem 71-jährigen Patienten mit Diabetes mellitus Typ 2, Grpßmann et al., Internist (Berl). 2021; 62(6): 672–678.
- [2]Euglycemic Diabetic Ketoacidosis: A Predictable, Detectable, and Preventable Safety Concern With SGLT2 Inhibitors, Rosenstock et al., Diabetes Care. 2015 Sep;38(9):1638-42. doi: 10.2337/dc15-1380.
Begeisterter Anästhesist mit Faible für Teaching und Medizininformatik.






4 Kommentare
Zum Kommentar-Formular springen
Danke für den tollen Artikel. Selbst auch schon mehrfach auf Intensiv beobachtet, immer im Zusammenhang mit Jardiance, einem meiner Meinung nach gefährlichem Medikament. Dieses wird ja auch gerne nicht-Diabetikern im Rahmen einer Herzinsuffizienztherapie verordnet
sehr cooler Artikel, ich hatte auch schon so einen ähnlichen Fall!
Bezüglich des Calcium würde ich immer das Albumin dazu bestimmen und das korrigierte Calcium auszurechnen, danach kann man über eine Substitution nachdenken.
Macht weiter so
Sehr schön, vielen Dank
Hey.
Ich habe schon Mal nach Operation so ein Patient gesehen. Ich denke viele noch nicht wissen, wie soll man mit SGTL-2-Inhibitoren umgehen.
Sehr gutes Artikel dazu:
https://www.akdae.de/arzneimittelsicherheit/bekanntgaben/newsdetail/atypische-diabetische-ketoazidosen-im-zusammenhang-mit-sglt-2-hemmern-gliflozine-aus-der-uaw-datenbank